Therapieoptimierung bei Biologika am Beispiel Secukinumab (Cosentyx)
1.11.2020, überarbeitet 03.11.2022, 8.11.2022 unter 3.6 ergänzt
Argumente und Ansatzpunkte für eine individuelle Therapieoptimierung
Inhaltsverzeichnis:
1. Jeder Mensch ist verschieden - Multikausalität der Psoriasis
2. Mögliche Vorteile einer individuellen Therapieoptimierung
3. Ansatzpunkte für eine individuelle Therapieoptimierung
3.1 Wiederholung der Initialdosierung oder (erneute) Stoßtherapie
3.2 Spritzenabstand
3.3 Einzelspritze mit 150 mg alle zwei Wochen
3.4 Dosisanpassung nach klinischem Bild (Haut- und/oder Gelenkzustand) und bedarfsgerechte Behandlung
- SCULPTURE Studie mit 150 und 300 mg Secukinumab
3.5 Wirkung-/Nebenwirkungs-Kompromiss
3.6 Dosisanpassung/-abstufung nach Körpergewicht
3.7 Dosisanpassung nach Laborwert
3.8 Kombination mit anderen Arzneimitteln
4. Risiken einer individuellen Therapieoptimierung
5. Links zu weiteren Informationen
1. Jeder Mensch ist verschieden - , selbst eineiige Zwillinge. Auch die Ursachen der Psoriasis sind unterschiedlich. Wenn vielleicht nicht von Mensch zu Mensch, so gibt es aber doch mehrere Arten der Erkrankung und die Psoriasis ist eine multifaktorielle Erkrankung. Dies äußert sich z.B. in mehreren Genabschnitten der DNA, die man mit der Psoriasis in Verbindung bringt. Die Faktoren können in unterschiedlicher Kombination und die auslösenden und/oder begünstigenden Umweltfaktoren in unterschiedlicher Intensität für die Psoriasis verantwortlich sein.
Allein schon bei nur vier Einflussgrößen, hier als a, b, c und d bezeichnet, ergeben sich (ohne Berücksichtigung der Reihenfolge)
14 Kombinationsmöglichkeiten:
a (nur alleine die Größe a, z. B. die Genveränderung a, ist bei einer Person vorhanden)
b
c
d
ab (z. B. die Genveränderungen a und b sind bei der Person vorhanden)
ac
ad
bc
bd
abc
abd
acd
bcd
abcd (z. B. gleich (alle) vier Genveränderungen sind bei der Person vorhanden)
Aus der Multikausalität der Psoriasis und unterschiedlichen Stoffwechselgegebenheiten bei Betroffenen sowie verschiedenen Lebensumständen folgt eine große Anzahl unterschiedlicher Reaktionen auf eine (standardisierte) Therapie, das heißt ein verschiedenes Ansprechverhalten und auch unterschiedliche und verschieden starke Nebenwirkungen.
Dies zeigt sich deutlich in den Studienergebnissen, bei denen die Wirksamkeit in der Regel sehr weit von 100 % entfernt ist und 80 % Ansprechrate schon ein sehr guter Wert wäre.
Die oben beschriebenen individuellen Gegebenheiten beim einzelnen Patienten kann die arzneimittelherstellende Industrie kaum, der behandelnde Arzt ein wenig und ein erfahrener Dermatologe könnte sie etwas mehr berücksichtigen und die Therapie entsprechend anpassen. Umso mehr ist der einzelne, erfahrene und mündige Patient selbst gefragt und in der Verantwortung.
2. Mögliche Vorteile einer individuellen Therapieoptimierung
Durch eine auf den einzelnen Patienten angepasste Therapie könnten
- ·die Wirksamkeit der Behandlung verbessert werden
- ·unerwünschte Nebenwirkungen verringert oder vermieden werden
- ·unter Umständen die Therapiekosten herabgesetzt werden
- ·die Patienten Compliance sich verbessern
- ·die Dauer der Wirksamkeit des Biologikums verlängert (ein Wirkverlust verhindert) werden
3. Ansatzpunkte für eine individuelle Therapieoptimierung
3.1 Wiederholung der Initialdosierung oder (erneute) Stoßtherapie
Eine Betrachtung der Pharmakokinetik von Secukinumab bei dem vom Hersteller vorgegebenen Therapieschema (zu Anfang fünf Dosen im Abstand von einer Woche, dann alle vier Wochen eine „Erhaltungsdosis“) zeigt, dass theoretisch ca. vier Wochen nach Therapiebeginn die maximale Serumkonzentration von Secukinumab vorliegt (vgl. Cosentyx® Initialdosierung, Aufdosierung bzw. Stoßtherapie - zeitlicher Verlauf der Secukinumab-Menge im Körper - Cosentyx® - Erfahrungen und Überlegungen zur Therapie mit Secukinumab - Psoriasis-Netz ).
Der Spitzenwert (etwa 3,5) zu Behandlungsbeginn nach vier Wochen liegt um rund 75 % höher als der Spitzenwert der „Erhaltungsdosis“ nach 28 Wochen (rund 2).
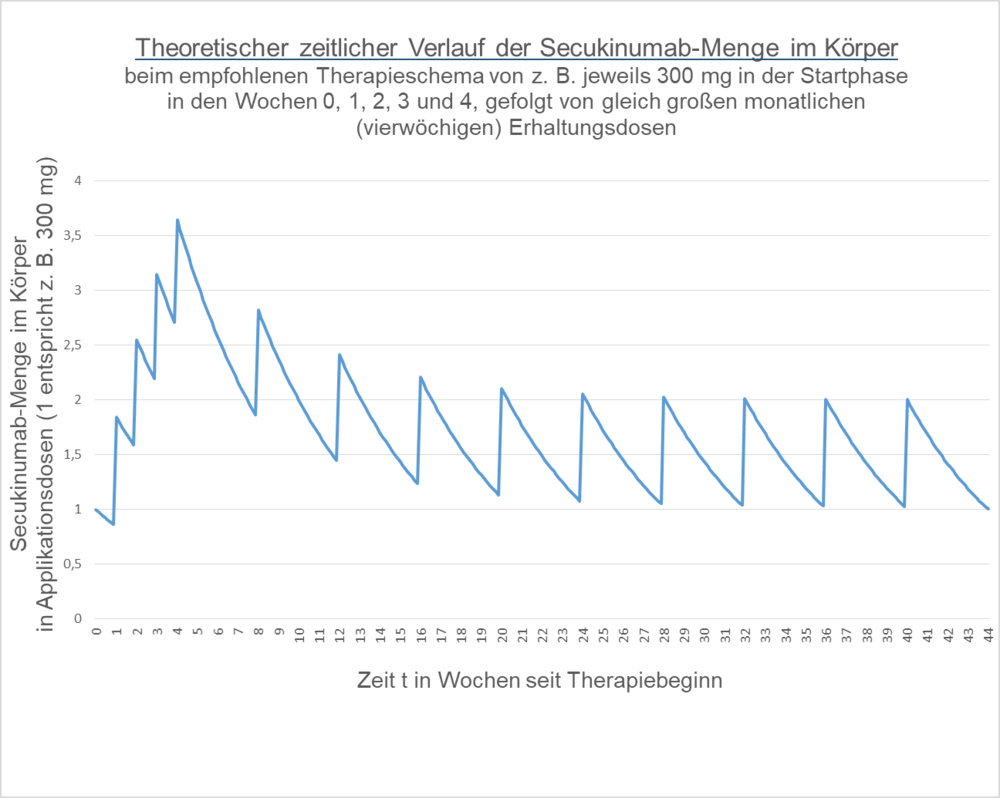
Das obige Diagramm geht von einer Reihe vereinfachender Annahmen aus, die nicht der menschlichen Physiologie entsprechen. So wird stark vereinfachend angenommen, dass die gesamte gespritzte Antikörpermenge augenblicklich sich im Körper verteilt. Tatsächlich wird individuell unterschiedlich schnell und unterschiedlich viel gespritztes Secukinumab aus dem Fettgewebe des Bauches oder des Oberschenkels in das Serum überführt.
Überlegenswert ist, bei Verschlechterung des klinischen Psoriasisbildes, eine erneute „Stoßtherapie“ durchzuführen ähnlich wie zu Therapiebeginn. Da ja bereits eine gewisse Menge Secukinumab im Serum enthalten ist, würden nun etwa drei im Abstand einer Woche applizierte Dosen ausreichen, um den anfänglichen Spitzenwert (3,5) erneut zu erreichen.
3.2 Spritzenabstand
Bei gutem Ansprechen auf die Therapie oder bei unerwünschten Nebenwirkungen könnte, über eine Verlängerung des Spritzenintervalls über vier Wochen hinaus, die mittlere Serumkonzentration von Secukinumab verringert werden.
3.3 Einzelspritze mit 150 mg alle zwei Wochen
Statt alle vier Wochen sich zwei Spritzen mit je 150 mg Secukinumab sich zu spritzen, könnte auch alle zwei Wochen eine Spritze mit 150 mg gespritzt werden. Die Konzentration von Secukinumab im Serum wäre dann geringeren Schwankungen unterworfen. Die „Zähne“ der „Sägezahnkurve“ wären kleiner, die Spitzenwerte somit geringer und die Minimalwerte der Serumkonzentration vor der nächsten Injektion wären angehoben.
3.4 Dosisanpassung nach klinischem Bild (Haut- und/oder Gelenkzustand)
und bedarfsgerechte Behandlung
Da Secukinumab auch bei geringerer Erhaltungs-Dosierung als 300 mg alle vier Wochen ausreichend wirken kann, ist eine Dosierung nach dem Hautzustand gut vorstellbar.
Laut der SCULPTURE Studie („Secukinumab retreatment-as-needed versus fixed-interval maintenance regimen for moderate to severe plaque psoriasis: A randomized, double-blind, noninferiority trial (SCULPTURE)“) ist die Nicht-Unterlegenheit einer bedarfsgerechten Behandlung im Vergleich zu einer Behandlung mit festen Intervallen bei 300 mg und 150 mg nicht nachgewiesen. Allerdings ist der Prozentsatz der Personen, die bei einer bedarfsgerechten Behandlung den PASI 75 beibehielten, mit 67,7 % (bei 300 mg) und 52,4 % (bei 150 mg) jeweils nur rund 10 % geringer als bei der Behandlung mit festen Intervallen (vgl. folgende Abb. 4. der SCULPTURE Studie).
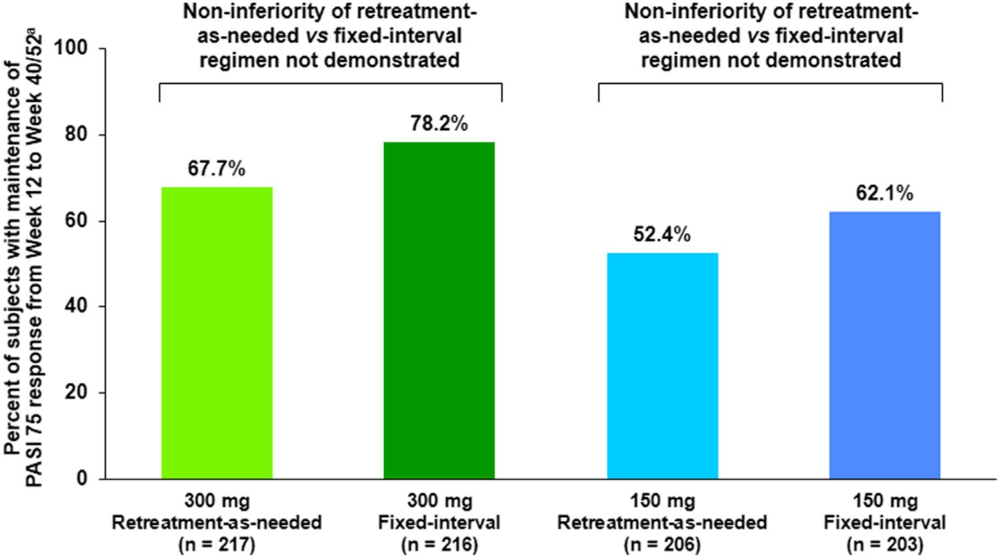
Abbildung 4. Beibehaltung einer Verbesserung von 75 % oder mehr gegenüber dem Ausgangswert des Psoriasis Area and Severity Index (PASI 75). Dargestellt sind die Prozentanteile der Personen, die in Woche 12 mit PASI 75 ansprachen und zwischen der 40. und 52. Woche beibehielten, bei einer bedarfsgerechten Behandlung im Vergleich zu einer Behandlung mit festen Intervallen bei 300 mg und 150 mg. Ergänzende Abb. 1 (verfügbar unter http://www.jaad.org) veranschaulicht den statistischen Vergleich der Nicht-Unterlegenheit zwischen den Schemata für diesen Endpunkt. n = Anzahl auswertbarer Patienten. aDas Ansprechen von PASI 75 wurde bei Patienten mit dem Fest-Intervall-Schema in Woche 52 beurteilt; bei Patienten mit einer bedarfsgerechten Behandlung wurde das Ansprechen von PASI 75 bei denjenigen, die in Woche 40 eine aktive Behandlung benötigten, in Woche 52 beurteilt, bzw. in Woche 40 bei denjenigen, die in Woche 40 keine aktive Behandlung benötigten.
Originaltext:
Fig 4. Maintenance of 75% or more improvement from baseline Psoriasis Area and Severity Index score (PASI 75) response. The proportions of week-12 responders who maintained PASI 75 response between weeks 40 and 52 for retreatment-as-needed versus fixed-interval treatment regimens at 300 mg and 150 mg are shown. Supplementary Fig 1 (available at http://www.jaad.org) illustrates the statistical noninferiority comparison between regimens for this end point. n = number of evaluable patients. aMaintenance of PASI 75 response was assessed at week 52 for patients on the fixed-interval regimen; for patients on the retreatment-as-needed regimen, PASI 75 response was assessed at week 52 for those who required active treatment at week 40, or at week 40 for those who did not require active treatment at week 40.
------------------------------------------------------------------------------------------------------------------------
Die obige Abbildung 4 veranschaulicht zudem, dass bereits bei einer Dosierung von 150 mg, also der Hälfte der laut Beipackzettel vorgegebenen Dosis von 300 mg bei Plaque Psoriasis, bei einem großen Anteil der Personen vergleichbare Behandlungserfolge erzielt werden.
Bei der bedarfsgerechten Behandlung mit 150 mg sind dies nach Abbildung 4 immerhin 52,4 % (gegenüber 67,7 % bei 300 mg – nur 15,3 % mehr) und bei festen Intervallen 62,1 % (gegenüber 78,2 % bei 300 mg).
Bei 52,4 %, bzw. 62,1 % der Personen stellt somit eine Behandlung mit 300 mg eine unnötig hohe Dosierung von Secukinumab dar.
Bei Gelenkbeteiligung ist mit längeren Zeitspannen für das Krankheitsgeschehen zu rechnen und oft eine sogenannte Basistherapie erforderlich. Therapieänderungen erfordern meiner Meinung nach daher hier mehr Umsicht und Fingerspitzengefühl und wollen besonders gut überlegt sein.
3.5 Wirkung-/Nebenwirkungs-Kompromiss
Bei einer niedrigeren Dosierung von Secukinumab können sich sowohl unerwünschte Nebenwirkungen, wie auch die erwünschte Wirkung, reduzieren.
Der Patient könnte zusammen mit dem Arzt seines Vertrauens die Dosierung so anpassen, dass sich der für den Patienten optimale, gewünschte Kompromiss zwischen Wirkung und unerwünschten Nebenwirkungen einstellt bei einem für den Patienten zufriedenstellenden PASI.
3.6 Dosisanpassung/-abstufung nach Körpergewicht
Nach der Initialdosierung beträgt laut der Fachinformation (Juni 2022 V007) die empfohlene Erhaltungsdosis für Erwachsene bei Plaque-Psoriasis 300 mg Secukinumab monatlich (dies kann z.B. bedeuten alle vier Wochen, d.h. alle 28 Tage, oder z.B. immer am ersten eines Monats, d.h. je nach Monatslänge alle 28 bis 31 Tage).
"Basierend auf dem klinischen Ansprechen kann eine Erhaltungsdosis von 300 mg alle 2 Wochen einen zusätzlichen Nutzen für Patienten mit einem Körpergewicht von 90 kg oder mehr bieten.", heißt es in der Fachinformation.
Wie ist nun ein Patient mit einem Körpergewicht von 89 kg optimal zu behandeln?
In welchem Rahmen können und dürfen behandelnde Ärzte die empfohlene Erhaltungsdosis nach eigenem Ermessen entsprechend dem klinischen Ansprechen und dem Körpergewicht der Patienten anpassen und optimieren?
Bei Kindern mit Plaque-Psoriasis wird bei der Behandlung mit Secukinumab nach drei Gewichtsklassen unterschieden und zudem bei einem Gewicht von größer oder gleich 50 kg neben der Dosis von 150 mg auch auf einen möglichen zusätzlichen Nutzen einer 300 mg Dosis hingewiesen.
Wäre hier denn auch eine Dosierung von 225 mg ( Injektionen mit 150 mg und 75 mg) eine weitere "zulässige" Dosierungsabstufung?

Quelle: https://klinischeforschung.novartis.de/dokumente/fachinformationen-cosentyx-150-mg-300-mg-injektionsloesung-in-einem-fertigpen-und-in-einer-fertigspritze/ , abgerufen 10.10.2022
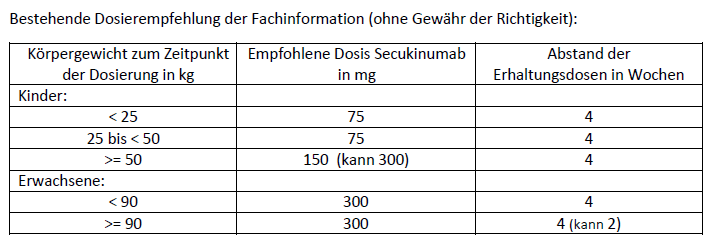
Im Folgenden eine Tabelle mit einem Diskussionsvorschlag für eine an das Körpergewicht der Person angepasste Dosierung. Gewählt wurde teilweise eine gewichtsproportionale Abstufung der Dosierung. Insgesamt ist die Tabelle nicht durchgehend systematisch aufgebaut, sondern enthält „Brüche“, die zeigen, dass ausgehend von unterschiedlichen „Fixpunkten“ sich für ein Körpergewicht verschiedene Dosierungen in der Inter-, bzw. Extrapolation ergeben können.
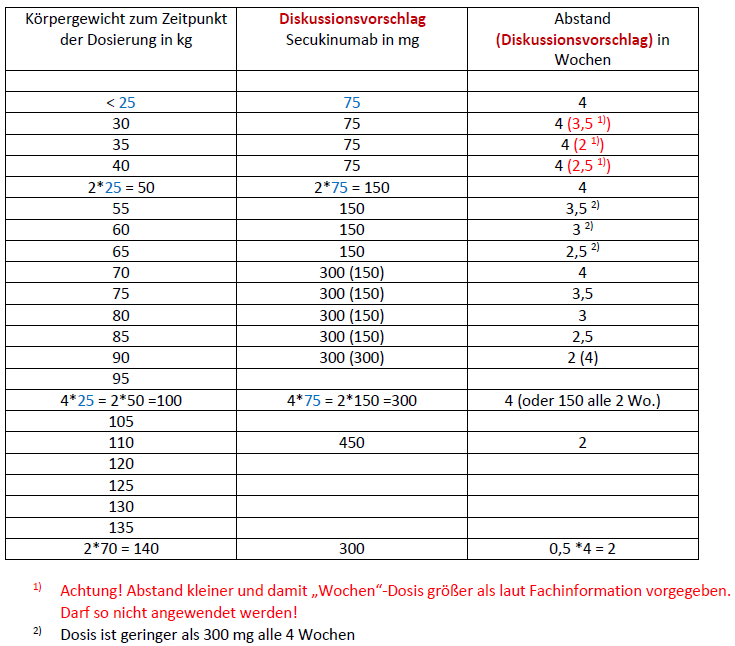
Eine Dosierung, alleine am Körpergewicht ausgerichtet, wird jedoch im Allgemeinen nicht ein optimales Ergebnis bringen. Vielmehr sind außer dem Körpergewicht viele weitere individuelle Faktoren der Pharmakokinetik und -dynamik relevant, z.B. Körpervolumen/-zusammensetzung, Serum-Interleukin-Spiegel, Abbau, Ausscheidung, Krankheits-/Entzündungsaktivität…
3.7 Dosisanpassung nach Laborwert
Ideal wäre es, die Secukinumab-Gaben an dem Interleukin 17A Plasmaspiegel des Patienten auszurichten. So wird z. B. bei Diabetes die zu spritzende Insulinmenge nach einer Blutzuckerbestimmung festgelegt.
Denkbar ist auch eine Bestimmung des Secukinumab-Spiegels im Blut, ähnlich wie es bei einigen Psychopharmaka zur Kontrolle des Medikamentenspiegels im Blut und der Anpassung des Dosierschemas durchgeführt wird.
Laut Cosentyx® Fachinformation wurde in einigen Studien die Secukinumab-Konzentration im Blut zur Untersuchung der Pharmakokinetik bestimmt.
3.8 Kombination mit anderen Arzneimitteln
Secukinumab kann zusammen mit topischen (äußerlich angewendeten) Arzneimitteln, wie z. B. den sogenannten Vitamin D haltigen Cremes und Salben angewendet werden.
... ist zu ergänzen
4. Risiken einer individuellen Therapieoptimierung
Sofern die empfohlene Medikamentendosis verringert wird, sind zu den im Beipackzettel genannten unerwünschten Nebenwirkungen, keine zusätzlichen Nebenwirkungen zu erwarten.
Im Gegenteil ist eher zu erwarten, dass sich Nebenwirkungen verringern. Dies kann allerdings auf Kosten der erwünschten Wirksamkeit gehen.
Zu klären ist, ob eine individuelle Therapieoptimierung als sogenannter „off label use“ von Cosentyx® angesehen wird und sich daraus Konsequenzen für die Kostenübernahme durch die Krankenkasse und/oder Beihilfe ergeben.
Ist das Ansprechen auf die Secukinumab-Dosis nach einer längeren Pause schlechter oder verliert das Biologikum seine Wirkung?
5. Links zu weiteren Informationen
Medizin nach Maß - Schuppenflechte - Psoriasis-Netz
#######################################################################################
Links in Überarbeitung:
"Cosentyx® - Dosierung, Halbwertszeit und pharmakokinetische Eigenschaften":
https://www.psoriasis-netz.de/community/blogs/entry/4075-cosentyx®-dosierung-halbwertszeit-und-pharmakokinetische-eigenschaften/
Übersicht der in der Fachinformation genannten Studien zu Secukinumab in meinem Blog "Cosentyx® (Secukinumab) - Studien zur Therapie der Plaque-Psoriasis, ankylosierender Spondylitis, Psoriasis bei Kindern - eine Übersicht":
https://www.psoriasis-netz.de/community/blogs/entry/4066-cosentyx®-secukinumab-studien-zur-therapie-der-plaque-psoriasis-ankylosierender-spondylitis-psoriasis-bei-kindern-eine-übersicht/
Siehe auch meinen Blog-Beitrag "(Secukinumab) - individuelle Erhaltungsdosis finden!?":
https://www.psoriasis-netz.de/community/blogs/entry/4062-cosentyx®-secukinumab-individuelle-erhaltungsdosis-finden/
bearbeitet von GrBaer185
-
 1
1
-
 1
1



5 Kommentare
Empfohlene Kommentare
Erstelle ein Benutzerkonto oder melde dich an, um zu kommentieren
Du musst ein Benutzerkonto haben, um einen Kommentar verfassen zu können
Benutzerkonto erstellen
Neues Benutzerkonto für unsere Community erstellen. Es ist einfach!
Neues Benutzerkonto erstellenAnmelden
Du hast bereits ein Benutzerkonto? Melde dich hier an.
Jetzt anmelden